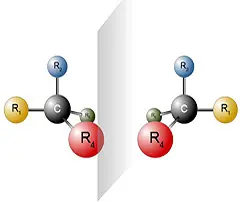
Welche Möglichkeiten gibt es Enantiomere via HPLC zu trennen?
- Der mobilen Phase wird "Chiralität zugeführt" - z. B. durch Zusatz eines chiralen Reagens. Dadurch entstehen zwischen den Probemolekülen und den Molekülen des chiralen Reagens diastereomere Komplexe, die unterschiedlich schnell durch die Trennsäule wandern. Die stationäre Phase bleibt dabei unverändert, d. h. sie ist achiral.
- Die Enantiomere werden reversibel mit einer geeigneten chiralen Verbindung derivatisiert, d. h. chemisch umgesetzt. Dadurch entstehen Diastereomere, die sich auf herkömmlichen HPLC Phasen trennen lassen. Nach erfolgter Trennung werden die Derivate wieder gespalten, wobei darauf zu achten ist, dass unter den Reaktionsbedingungen keine Racemisierung auftritt.
- Als stationäre Phase wird eine speziell modifizierte, chirale Phase verwendet. Die mobile Phase bleibt unverändert. Die zu trennenden Enantiomere treten unterschiedlich stark mit der chiralen stationären Phase in Wechselwirkung und verlassen somit zu unterschiedlichen Zeiten die Trennsäule.
Die letzte der genannten Möglichkeiten (Nummer 3) wird im Allgemeinen als "chirale HPLC" bezeichnet. Sie ist von den drei Varianten am einfachsten durchzuführen und die Wahrscheinlichkeit für eine erfolgreiche Trennung ist - aufgrund der Vielzahl an erhältlichen stationären Phasen - fast garantiert.
Welche stationären Phasen werden für die chirale HPLC verwendet?
Die stationären Phasen für die chirale HPLC (engl.: Chiral Stationary Phases - CSPs) basieren mehrheitlich auf Silika-Gel. Um Enantiomere zu trennen wird dieses mit sogenannten chiralen Selektoren modifiziert. Bis heute wurden eine Vielzahl von solchen Verbindungen entwickelt, wodurch die Auswahl an erhältlichen Phasen enorm groß ist.
Folgende Verbindungsklassen werden hauptsächlich als chirale Selektoren verwendet:
- Sogenannte "Bürstenphasen" - Einfache chirale Moleküle, die ähnlich der Alkylketten bei der RP-HPLC, auf die Oberfläche des Silica-Gels gebunden sind, z. B. Dinitrobenzoylphenylglycin
- Helicale Polymere, z. B. Cellulose– oder Amylosederivate
- Chirale Käfigverbindungen, z. B. Cyclodextrine oder Kronenether
- Proteine, z. B. Rinderserumalbumin (BSA) oder Pepsin
- Ligandenaustauschphasen, z. B. Aminosäure-Kupfer-Komplexe
Am meisten werden modifizierte Cellulose– oder Amylosederivate verwendet, weil mit diesen Phasen im Vergleich zu anderen chiralen Selektoren eine sehr großes Spektrum an Enantiomeren getrennt werden kann.
Wie werden die chiralen Selektoren an das Silica-Gel gebunden?
Dafür gibt es mehrere Möglichkeiten. Einige der chiralen Selektoren können kovalent an das Silica-Gel zu gebunden werden. Für manche der chiralen Selektoren ist dies aber nicht möglich. So werden z. B. Polysaccharidderivate in einem speziellen Verfahren entweder an das Silica-Gel chemisch immobilisiert ("Immobilized CSPs") oder darauf beschichtet ("Coated CSPs"). Der Unterschied zwischen den "Immobilized CSPs" und den "Coated CSPs" besteht darin, dass die immobilisierten Phasen gegenüber organischen Lösungsmittel weitaus robuster sind. Für die Coated CSPs sind eine Reihe von Lösungsmitteln nicht erlaubt, da diese die chirale stationäre Phase mit der Zeit unbrauchbar machen. Für die "Immobilized CSPs" ist das nicht der Fall, was die Methodenentwicklung für die Trennung von Enantiomeren vereinfacht.
Welche mobile Phasen können für chirale Trennungen verwendet werden?
Das ist abhängig von der stationären Phase. Wie oben bereits erwähnt gibt es chirale Phasen, die mit sehr vielen organischen Lösungsmitteln kompatibel sind und wieder andere bei denen die Anzahl an möglichen Eluenten sehr limitiert ist. Welche Eluenten verwendet werden dürfen, findet man oft in den mitgelieferten Säuleninfo- bzw. "Care&Maintanance"-Sheets der Hersteller. Falls Unsicherheit besteht, sollte beim jeweiligen Hersteller oder Händler nachgefragt werden.
Weitere Tipps und Informationen zur chiralen Chromatographie
Chirale Trennungen werden in der Regel isokratisch durchgeführt. Wie bei anderen chromatographischen Verfahren auch, ist die Auflösung für ein bestimmtes Analytpaar stark von der Selektivität der stationären Phase abhängig. Zwei weitere wichtige Parameter für die Methodenentwicklung sind die mobile Phase und die Temperatur. Bei chiralen Trennungen ist es oft der Fall, dass mit sinkender Temperatur die Auflösung steigt.